Command Palette
Search for a command to run...
AI 驱动从头设计多样化小分子结合蛋白,韩国团队发现能选择性识别压力激素的蛋白质

在生命科学与合成生物学领域,如何设计既具有高亲和力又具有高特异性的小分子结合蛋白,一直是实现生物传感与分子开关的关键挑战。过去,这一方向主要依赖对天然蛋白的筛选与改造,或基于既有蛋白骨架的物理建模设计,通用性与可扩展性始终受限。
针对于此,来自韩国科学技术院(KAIST)生物科学系的研究团队借助深度学习驱动的蛋白结构生成与序列设计方法,以 NTF2 样折叠(NTF2-like fold)为核心「通用 backbone」,从头设计(de novo)多样化的小分子结合蛋白,并进一步将其转化为类似化学诱导二聚化(CID)的传感器。研究人员成功设计了一种能够选择性识别压力激素皮质醇的蛋白质,并基于此开发了一种人工智能生物传感器。该案例超越了蛋白质设计本身,迈向了可实际测量的传感器技术,解决了蛋白质设计领域长期存在的小分子识别难题。
相关研究成果以「Small-molecule binding and sensing with a designed protein family」为题,已刊登 Nature Communications 。
研究亮点:
* 利用人工智能从头设计(de novo)识别特定化合物的蛋白质,并将其应用于功能性生物传感器
* 传统方法主要涉及寻找天然蛋白质或修改其某些功能,而本研究则通过基于人工智能的设计「定制」了具有所需功能的蛋白质
* 研究成果可广泛应用于疾病诊断、新药研发和环境监测等领域

论文地址:
https://www.nature.com/articles/s41467-026-70953-8
更多 AI 前沿论文:
https://hyper.ai/papers
数据集:构建 NTF2 backbone
为实现设计目标,研究人员首先通过家族级「幻觉(hallucination)」方法生成了一组 NTF2 结构(集合 1:1,615 个 backbones),随后利用 ProteinMPNN 对这些骨架进行序列重新设计,并通过 AlphaFold 筛选出能够折叠成设计结构的蛋白(集合 2:3,230 个 backbones)。此外,其还利用 Rosetta 参数化生成骨架结构,并同样通过 ProteinMPNN 进行序列设计,再使用 AlphaFold 进行结构验证(集合 3:6,838 个 backbones),见下图:
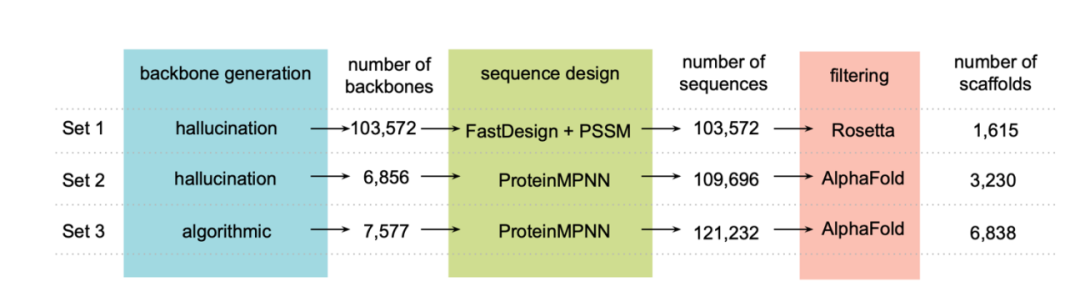
最终,经过筛选后,研究人员还获得了用于实验表征的编码寡核苷酸,其中包括:630 个 HCY 结合蛋白、 1,661 个 ROC 结合蛋白、 16,276 个 WRF 结合蛋白、 9,024 个 APX 结合蛋白、 19,390 个 IRI 结合蛋白以及 7,573 个 OHP 结合蛋白。
设计具有多样化口袋几何结构的 NTF2 蛋白家族
NTF2 折叠由 3 条 α 螺旋和一张弯曲的 6 股 β 折叠片构成,这些结构共同形成了该折叠家族所特有的大型内部结合口袋,如下图:
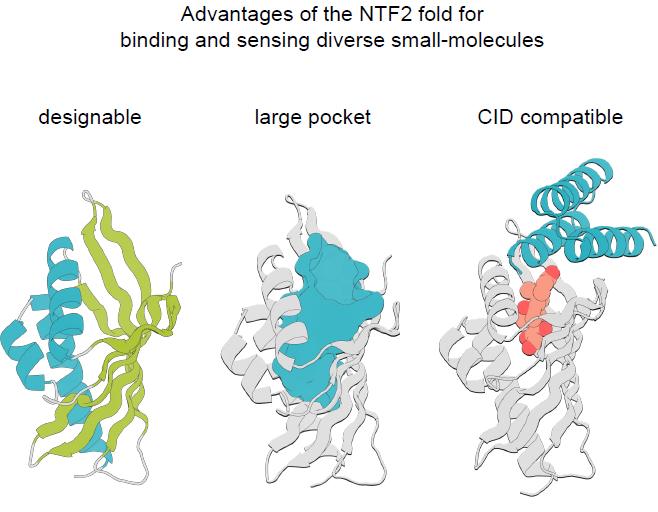
这种折叠在自然界中的多样性主要来源于较长且不规则的环区以及独特的四级结构,这两者都会影响结合口袋的几何形态和功能。本研究的目标是设计一类具有多样化口袋几何结构的 NTF2 蛋白家族,以容纳广泛的小分子,同时尽量减少环区以保持其模块化特性和可设计性,整体设计流程如下图所示:
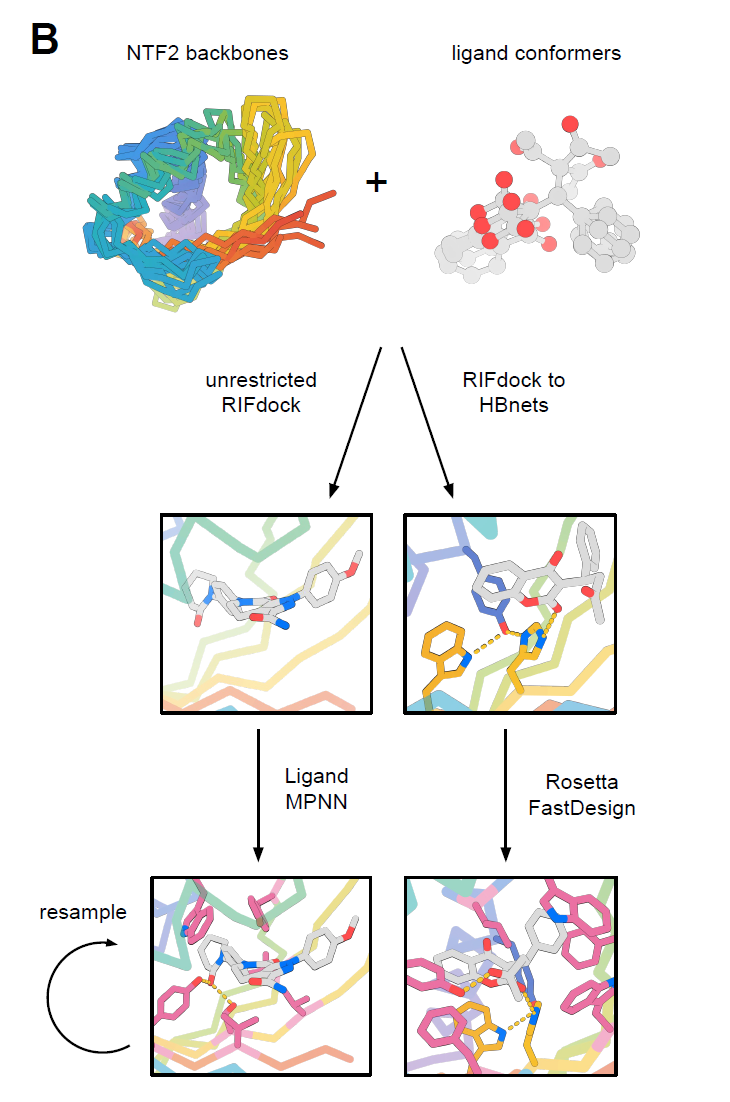
在获得超过 10,000 个具有多样口袋几何结构的 NTF2 设计蛋白后,研究人员使用 RIFdock 将 6 种在化学性质和结构上各不相同的小分子放置到这些骨架的中心口袋中。这些小分子包括应激激素皮质醇(HCY)、抗凝药华法林(WRF)、肌肉松弛剂罗库溴铵(ROC)、抗凝药阿哌沙班(APX)、来源于抗癌药伊立替康的抗肿瘤活性分子 SN-38(IRI),以及激素 17-α-羟基孕酮(OHP)。
在蛋白设计中,极性界面的构建是一项重要挑战,尤其对于小分子结合蛋白而言,需要在内部口袋中引入极性残基以与配体的极性官能团相互作用,同时又不能破坏蛋白的整体稳定性。为此,研究人员采用两种策略:
方法 1(RIFdock to HBNets)
研究人员将 HCY 、 WRF 、 ROC 、 APX 和 IRI 对接到集合 1 backbone 中,并要求至少存在一个由 HBNet 残基介导的蛋白–小分子相互作用,随后采用基于天然序列引导的 Rosetta 设计进行优化,其中利用来源于 NTF2 家族蛋白的位置特异性评分矩阵对序列设计进行偏置。
方法 2(unrestricted RIFdock)
使用无约束的 RIFdock 将 OHP 、 APX 和 IRI 放置到集合 2 和集合 3 的 backbone 中,并利用 LigandMPNN 进行序列设计。 LigandMPNN 是 ProteinMPNN 的一个变体,专门在蛋白–小分子复合物数据上训练,能够在设计过程中显式考虑配体的存在。
在筛选设计结果时,研究人员使用 Rosetta 计算蛋白–配体之间的氢键数量、结合能(ddG)以及接触分子表面积(CMS);对于方法 2,还结合单序列 AlphaFold 预测结果,筛选能够同时再现目标折叠结构及结合位点的设计(见下图)。
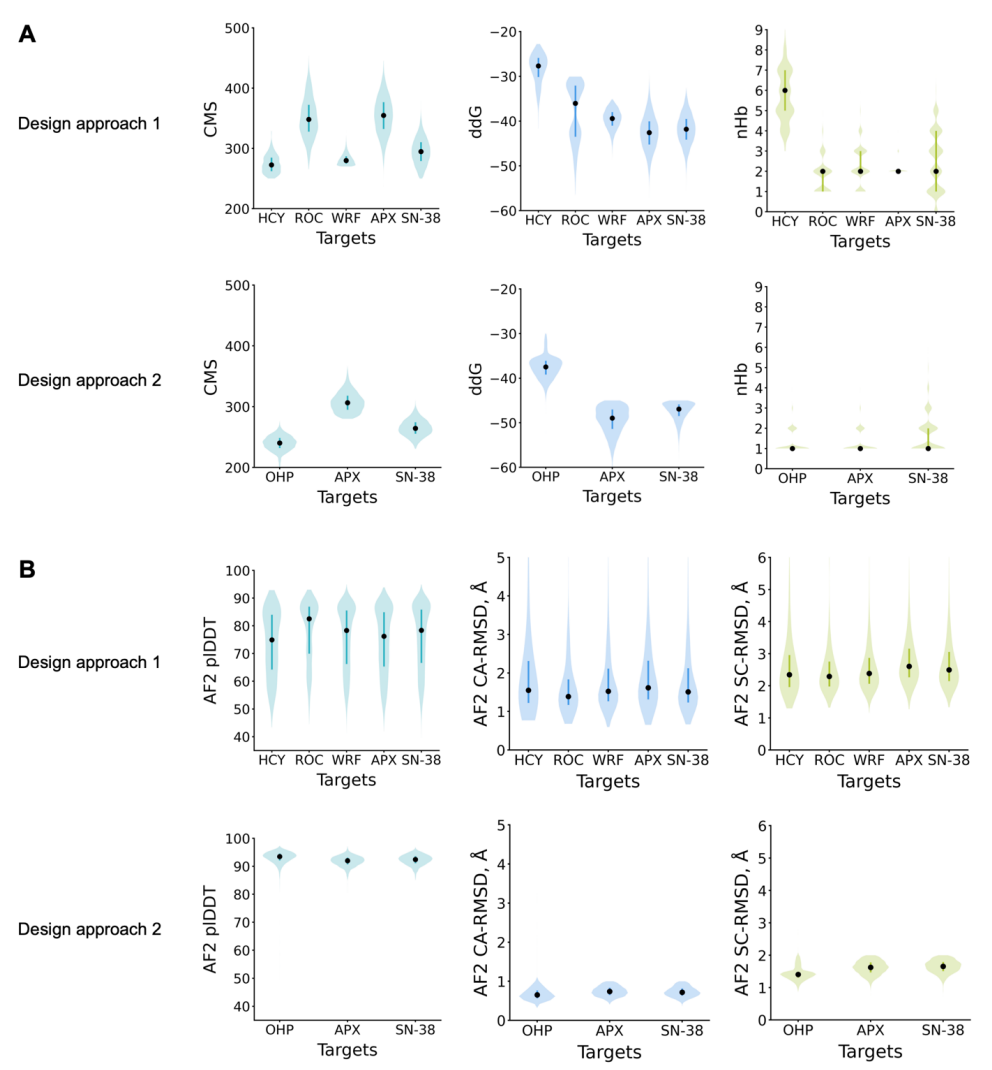
成果展示:基于 NTF2 的小分子结合蛋白可应用于生物传感器
研究人员设计了系列试验,来验证本研究提出的设计策略的有效性:
设计结合蛋白的结构表征
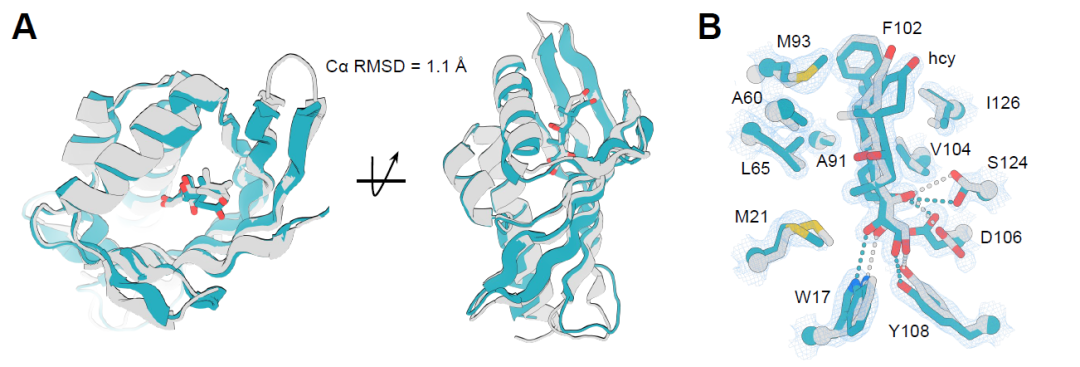
为验证设计的小分子结合蛋白的准确性,研究解析了两种蛋白–配体复合物的晶体结构:皮质醇结合蛋白 hcy129 与阿哌沙班结合蛋白 apx1049 。其中,通过 ProteinMPNN 对 hcy129 进行表面重设计以提升结晶性,成功获得其与皮质醇复合物的 1.5 Å 高分辨率结构。结构比对显示,其整体折叠与设计模型高度一致,Cα RMSD 为 1.1 Å(下图 A),关键氢键残基及配体构象也精确匹配(下图 B),表明预构建的氢键网络(HBNet)有效实现了极性相互作用的精准设计。
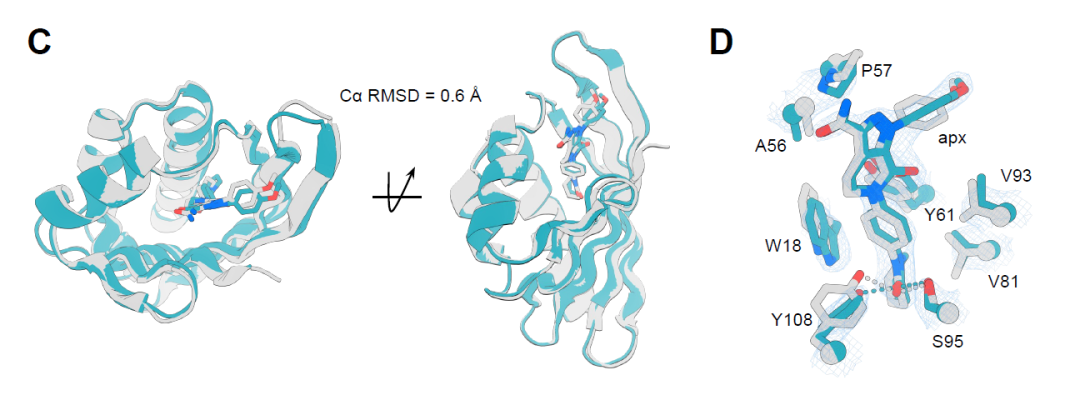
另一方面,apx1049 与阿哌沙班复合物的晶体结构分辨率为 2.1 Å,与设计模型一致性更高,在 113 个残基范围内的 Cα RMSD 仅为 0.6 Å(下图 C)。其蛋白–配体相互作用几乎完全复现设计,包括关键氢键及芳香残基间的 π–π堆积作用(下图 D),从而稳定配体构象并形成高度形状互补的结合口袋。这些结果证明了该设计策略在原子尺度上实现了高精度的蛋白–配体界面构建。
设计结合蛋白的特异性评估
为评估设计蛋白的特异性,研究对六种结合蛋白与六种配体进行了系统测试,并以具有非特异性结合能力的白蛋白作为对照。结果显示,hcy129.1 、 iri807.1 和 apx1049 等高亲和力蛋白在与各自靶标结合时,同时表现出良好的特异性,而白蛋白对多数配体几乎不发生结合,验证了设计策略的有效性。
此外,在华法林(WRF)体系中,白蛋白与其结合亲和力(KD 约 5.0 μM)与设计蛋白 wrf1071(KD 约 1.1 μM)相近,说明对于疏水性较强的配体,非特异性结合仍具挑战。
总体而言,该方法已能实现一定程度的高特异性识别,但在区分结构相似分子及提升对疏水性配体的选择性方面,仍有进一步优化空间。
生物传感器构建(皮质醇诱导异源二聚体的设计与表征)
皮质醇在生理样本中通常以低纳摩尔浓度存在,而当血浆皮质醇水平高于 38 nM 时,可作为库欣综合征等疾病的诊断依据。为提高 hcy129 对皮质醇的结合亲和力以用于生物传感,研究人员基于其单点饱和突变(SSM)实验中筛选出的有利突变构建了组合突变体文库,并通过酵母展示进行筛选,观察到结合亲和力显著提升,如下图所示:
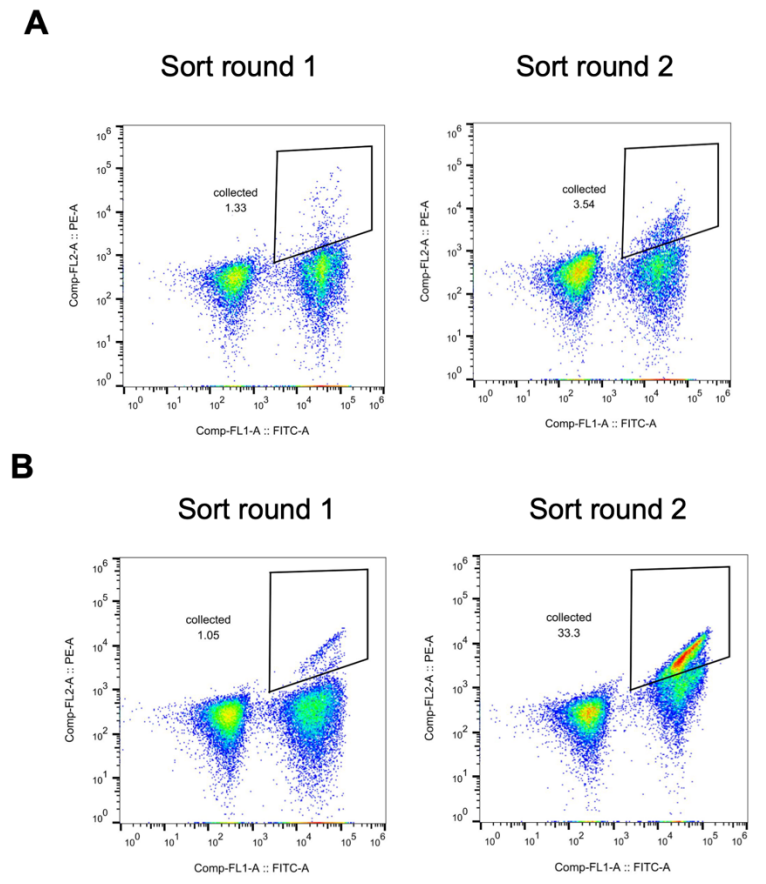
随后,研究人员从该文库中筛选出最佳变体,在大肠杆菌中表达并通过等温滴定量热(ITC)进行表征。该变体 hcy129.1 的 KD 为 68 nM,相较原始设计提高了 31 倍(如下图 C);结构分析表明,亲和力增强主要源于与皮质醇之间更强的疏水相互作用(下图 D)。
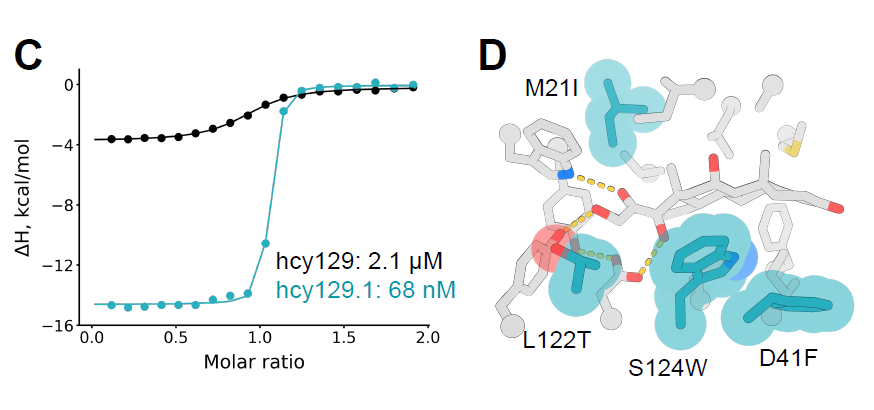
在此基础上,研究进一步设计皮质醇依赖的异源二聚体系。通过对 hcy129.1 结构进行改造并引入小型蛋白骨架,结合 RIFdock 、 Rosetta 与 ProteinMPNN 等方法进行计算设计与筛选,最终获得可与 hcy129.1 及皮质醇形成三元复合物的小型蛋白 miniH11 。
实验表明,该体系仅在皮质醇存在时形成稳定复合物。进一步地,研究将该体系与 NanoBiT 荧光素酶系统融合,实现皮质醇传感功能,检测到 EC50 约为 72 nM(下图 H),与结合亲和力一致,验证了设计的有效性。同时,体系在无皮质醇条件下亲和力显著降低,表明二聚作用具有良好的配体依赖性。
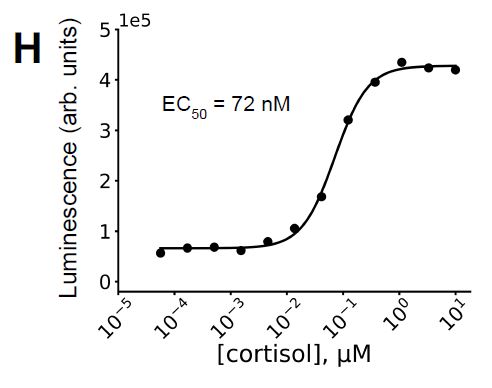
在等摩尔(200 nM)hcy129.1_CID-SmBiT 与 miniH11-LgBiT 体系中,皮质醇依赖的发光响应曲线
整体而言,该工作证明了基于 NTF2 的小分子结合蛋白可进一步工程化为功能性生物传感器。
结语
总体来看,这项研究为小分子结合蛋白的从头设计提供了一条全新路径:通过人工智能模型在原子层面精确刻画蛋白质–配体相互作用,实现了从「发现或改造天然蛋白」向「按需定制功能蛋白」的转变,并完成了实验层面的有效验证。
这不仅标志着蛋白质设计能力的跃迁,也显著拓展了其应用边界——从疾病早期诊断中的生物标志物精准检测,到新药研发中的靶向分子识别,再到环境监测中对污染物的实时感知。随着这一技术体系的不断成熟,具备高度特异性与可编程性的定制化生物传感器,有望成为连接生命科学与现实世界应用的重要桥梁。
参考文献:
https://www.nature.com/articles/s41467-026-70953-8
https://phys.org/news/2026-04-ai-proteins-built-specific-compounds.html